Ανεύρυσμα Κοιλιακής Αορτής
Τι είναι το ανεύρυσμα της κοιλιακής αορτής (ΑΚΑ) ;
Η αορτή είναι η μεγαλύτερη αρτηρία στο σώμα μας, και μεταφέρει το οξυγονωμένο αίμα από τη καρδιά μας στο υπόλοιπο σώμα. Το τμήμα αορτής που περνάει από το στήθος και το θώρακα ονομάζεται θωρακική αορτή, ενώ το τμήμα που βρίσκεται στην κοιλιά, ονομάζεται κοιλιακή αορτή. Ως ανεύρυσμα ορίζεται μια εντοπισμένη, παθολογική και μόνιμη διάταση του τοιχώματος ενός αγγείου, η οποία είναι τουλάχιστον 50% μεγαλύτερη από την αναμενόμενη φυσιολογική διάμετρό του. Η κανονική διάμετρος της κοιλιακής αορτής είναι περίπου 2 εκατοστά.
Όταν η αορτή πάσχει από ανευρυσματική νόσο τότε αυτή διατείνεται σε σημείο που να ξεπερνά τα 4 εκατοστά. Στις ΗΠΑ τα ραγέντα ΑΚΑ συνιστούν την 15η αιτία θανάτου στο γενικό πληθυσμό και την 10η σε άνδρες >55 ετών.1 Προκαλείται λόγω βλάβης ή μηχανικής αδυναμίας του αγγειακού τοιχώματος και μπορεί να οδηγήσει στη ρήξη του ανευρύσματος.
Η ρήξη του ανευρύσματος προκαλεί πολύ σοβαρή εσωτερική αιμορραγία. Στις περιπτώσεις αυτές ο ασθενής προσέρχεται με εικόνα κυκλοφορικής καταπληξίας (shock) και η θνητότητα προσεγγίζει ~ 70-80%.
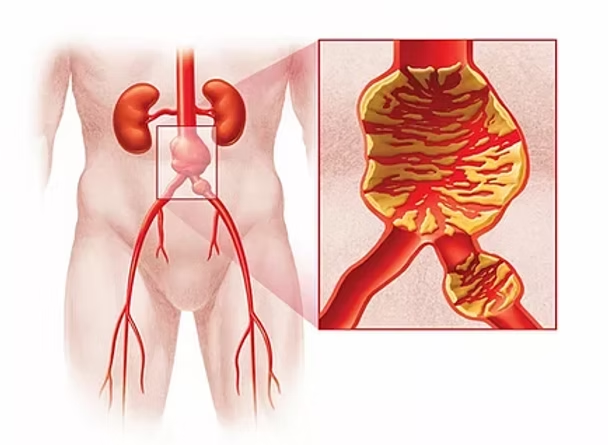
Παράγοντες που προκαλούν το ανεύρυσμα της κοιλιακής αορτής
Η αθηροσκλήρωση είναι ο κυριότερος παράγοντας κινδύνου για την ανάπτυξη της καρωτιδικής νόσου. Αθηροσκλήρωση είναι η συσσώρευση στην εσωτερική επιφάνεια των αρτηριών χοληστερόλης, λίπους, ασβεστίου και άλλων μεταβολικών προϊόντων, που σταδιακά σχηματίζουν την αθηρωματική πλάκα. Είναι συνήθως το αποτέλεσμα του καπνίσματος, της υψηλής αρτηριακής πίεσης (υπέρταση), της υψηλής χοληστερόλης (υπερχοληστερολαιμία) και της ηλικίας (>60 ετών). Η παχυσαρκία και ο διαβήτης συμβάλουν εξίσου στην εμφάνιση αθηροσκλήρωσης. Όλοι αυτοί οι παράγοντες, αυξάνουν σημαντικά τον κίνδυνο, δεν προκαλούν όμως κατ’ αναγκη και την ασθένεια. Για παράδειγμα άτομα με έναν ή περισσότερους παράγοντες κινδύνου ενδέχεται να μην προσβληθούν, ενώ αντίθετα, άτομα χωρίς εμφανείς παράγοντες κινδύνου μπορεί να νοσήσουν. Ο ρόλος των γονιδίων (οικογενειακό ιστορικό) είναι καθοριστικός.
Οι ασθενείς με καρωτιδική νόσο συχνά μπορεί να πάσχουν από στεφανιαία νόσο και περιφερική αρτηριακή νόσο καθώς και οι τρεις αυτές ασθένειες, έχουν σαν βάση την αθηροσκλήρωση και μοιράζονται τους ίδιους παράγοντες κινδύνου.
Εντόπιση και Συμπτώματα
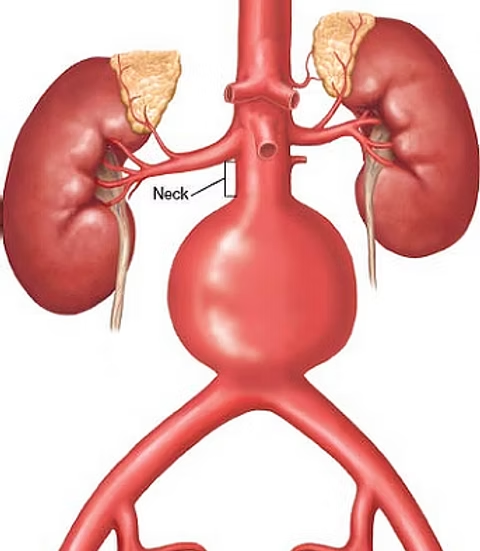
Τα ανευρύσματα της κοιλιακής αορτής εντοπίζονται κατά 95% κάτωθεν της εκφύσεως των νεφρικών αρτηριών. Είναι συνήθως ασυμπτωματικά και διαγιγνώσκονται τυχαία σε ελέγχους ρουτίνας ή κατά τη διάρκεια ελέγχου για άλλα νοσήματα. Το πιο συχνό εύρημα είναι ψηλαφητή διόγκωση και αίσθημα παλμών στην κοιλιά.
Καθώς αυξάνουν σε μέγεθος πιέζουν παρακείμενα όργανα, σπόνδυλους και νευρικές ρίζες προκαλώντας επιδεινούμενο σταδιακά πόνο στην κοιλιά ή τη μέση ή την πλάτη με αντανάκλαση στα πόδια, γλουτούς και βουβωνική περιοχή. Οι πόνοι αυτοί μπορούν λανθασμένα να εκληφθούν ότι οφείλονται σε δισκοπάθεια. Είναι δυνατόν να προκαλέσουν συμπτώματα από το γαστρεντερικό σύστημα, το ουροποιητικό σύστημα και από τα κάτω άκρα λόγω περιφερικού εμβολισμού (μπορεί να εμφανιστούν περιοχές με μπλε χρώμα και πόνο, λόγω εμβολής συντριμμάτων θρόμβου από το ανεύρυσμα). Όταν το ανεύρυσμα σπάσει, τότε τα συμπτώματα είναι: έντονος πόνος στην πλάτη ή την κοιλιακή χώρα, ωχρότητα, εικόνα σοκ, ρίγη, ναυτία, εμετός, ίλιγγος, λιποθυμία, ιδρώτας, έντονη ταχυκαρδία και ξαφνική αδυναμία.
Κίνδυνος Ρήξης και Αντιμετώπιση του ανευρύσματος κοιλιακής αορτής
Μικρού μεγέθους ανευρύσματα, διαμέτρου < 4-4.5 εκ., τα οποία δεν αυξάνονται ταχέως σε μέγεθος, ή που δεν προκαλούν συμπτωματολογία, έχουν μειωμένη πιθανότητα ρήξεως και συχνά δεν απαιτούν άλλη θεραπεία, παρά την τακτική παρακολούθησή τους. Αυτή περιλαμβάνει τη διενέργεια υπερηχογραφικού ελέγχου σε τακτά χρονικά διαστήματα για να καθοριστεί εάν και κατά πόσο το ανεύρυσμα έχει μεγαλώσει. Οι άνδρες καπνιστές με ηλικία άνω των 65 ετών και όσοι έχουν οικογενειακό ιστορικό πρέπει να υποβάλλονται σε υπερηχογράφημα κοιλίας. Παρόλο που δεν έχει τεκμηριωθεί η δράση φαρμάκων που να εμποδίζουν την ανάπτυξη του αορτικού ανευρύσματος, η ρύθμιση των παραγόντων κινδύνου – κάπνισμα, αρτηριακή υπέρταση, υπερλιπιδαιμία – προστατεύει από την ταχεία ανάπτυξη του ανευρύσματος.
Ο κίνδυνος ρήξης αυξάνεται σε ανεύρυσμα μεγαλύτερης διαμέτρου ενώ υπάρχει ένα όριο ( > 5.5 cm) πάνω από το οποίο ο ετήσιος κίνδυνος ρήξης αυξάνεται σημαντικά και ανέρχεται σε 10-15%. Ανευρύσματα με διάμετρο > 5.0-5.5 εκ. έχουν ένδειξη για χειρουργική αντιμετώπιση.
Η αντιμετώπιση του ανευρύσματος μπορεί να γίνει με ανοικτή χειρουργική επέμβαση ή ενδαγγειακά. Οι Dubost και Οικονόμου δημοσίευσαν το 1952 την πρώτη επιτυχή αποκατάσταση υπονεφρικού ανευρύσματος κοιλιακής αορτής με ανοικτή επέμβαση ΜΕ ομόλογο αρτηριακό μόσχευμα.2 Στις αρχές της δεκαετίας του 1990 οι Volodos και Parodi εισήγαγαν την ενδοαυλική (ενδαγγειακή) μέθοδο αποκατάστασης του ανευρύσματος κοιλιακής αορτής που σταδιακά κέρδισε μεγάλο χώρο στην αντιμετώπιση της πάθησης.3,4 Η ηλικία, οι συνυπάρχουσες παθήσεις και η κλινική κατάσταση του ασθενούς καθώς και οι μορφολογικές παράμετροι του ανευρύσματος θα πρέπει επίσης να λαμβάνονται υπόψη στην επιλογή της καταλληλότερης θεραπευτικής προσέγγισης.
Κλείσε ένα Ραντεβού
Συμπληρώστε τη φόρμα επικοινωνίας και θα σας καλέσουμε άμεσα για να ενημερωθούμε για τις ανάγκες σας, να απαντήσουμε σε όλες τις ερωτήσεις σας και να σας καθοδηγήσουμε στα επόμενα βήματα.
Ανοικτή Χειρουργική Επέμβαση
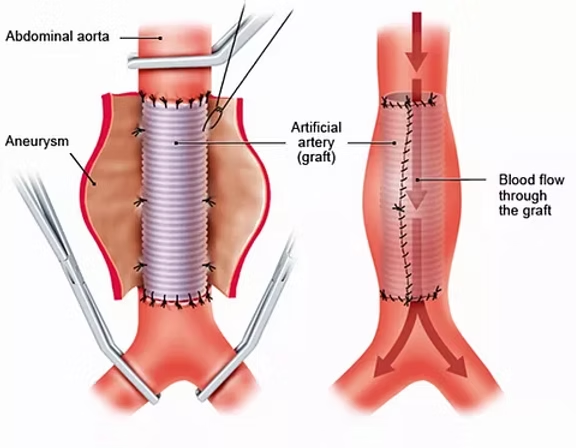
Η ανοιχτή επέμβαση περιλαμβάνει εκτομή του ανευρυσματικού σάκου και αποκατάσταση της συνέχειας της κοιλιακής αορτής με συνθετική πρόθεση. Η πρόθεση (μόσχευμα) είναι σωληνωτή, όταν περιορίζεται στην κοιλιακή αορτή, και διχαλωτή όταν επεκτείνεται και στις κοινές λαγόνιες αρτηρίες. Η κλασσική μέθοδος γίνεται υπό γενική αναισθησία και διαρκεί 2-4 ώρες. Μετά το χειρουργείο ο ασθενής παραμένει στο νοσοκομείο περίπου 1 εβδομάδα.
Ενδαγγειακή Αντιμετώπιση (EVAR)
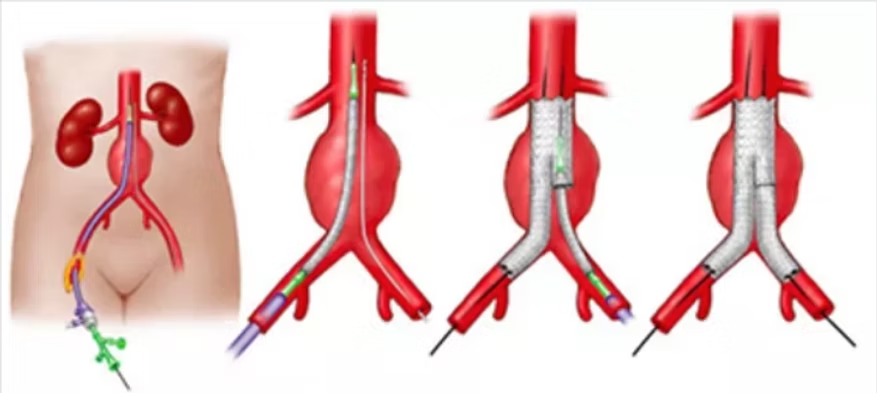
Η ενδαγγειακή αντιμετώπιση του ανευρύσματος της κοιλιακής αορτής, συνίσταται στην τοποθέτηση ενδοαυλικά ενός μοσχεύματος, το οποίο στηρίζεται σε μεταλλικό σκελετό (stent-graft). Η ενδαγγειακή επέμβαση μπορεί να διενεργηθεί με γενική, περιοχική ή τοπική αναισθησία και συνήθως για να ολοκληρωθεί απαιτείται μικρότερος χρόνος από την ανοικτή. Η ενδαγγειακή αποκατάσταση είναι σχετικά καινούργια μέθοδος και έγκειται στον αποκλεισμό του ανευρύσματος με ένα μόσχευμα το οποίο θα τοποθετηθεί στην αορτή μέσα από το αγγείο. Θα γίνουν δύο μικρές χειρουργικές τομές στις βουβωνικές περιοχές δεξιά και αριστερά. Με ειδικούς καθετήρες ο αγγειοχειρουργός μέσω των μηριαίων αρτηριών θα φτάσει στην κοιλιακή αορτή όπου και θα τοποθετήσει ένα ειδικό μόσχευμα μέσα από το αγγείο το οποίο θα αποκλείει το ανεύρυσμα από την κυκλοφορία. η διαδικασία αυτή απαιτεί πιο συχνή μετεγχειρητική παρακολούθηση του ασθενούς. Μετά το χειρουργείο ο ασθενής θα χρειαστεί να μείνει στο Νοσοκομείο για 3-4 ημέρες, και ο χρόνος ανάρρωσης είναι σημαντικά μειωμένος σε σχέση με την ανοιχτή μέθοδο. Ο ασθενής θα πρέπει να επισκεφτεί το αγγειοχειρουργό 2-3 φορές μέσα στο πρώτο χρόνο και να κάνει μία αξονική τομογραφία ή υπερηχοτομογράφημα για τον έλεγχο του μοσχεύματος.
Αποτελέσματα Μελετών και Σύγκριση των δύο Μεθόδων
Έως σήμερα 4 τυχαιοποιημένες κλινικές μελέτες έχουν διεξαχθεί προς αξιολόγηση των δύο μεθόδων (Χειρουργική αποκατάσταση: ΧΑ, και Ενδαγγειακή αποκατάσταση: ΕΑ). H μελέτη EVAR 1 πραγματοποιήθηκε μεταξύ Σεπτεμβρίου 1999 και Αυγούστου 2004 και συμπεριέλαβε 1252 ασθενείς σε 38 κέντρα του Ενωμένου Βασιλείου6-7. Η ολλανδική τυχαιοποιημένη μελέτη DREAM συμπεριέλαβε μεταξύ 2002 και 2008 345 ασθενείς (171 ΕΑ και174 ΧΑ) σε 24 κέντρα της Ολλανδίας και 4 του Βελγίου. 8 Η μελέτη OVER από τις ΗΠΑ συμπεριέλαβε 881 ασθενείς (>49 ετών), από 42 κέντρα, με ΑΚΑ, υποψήφιους και για τις δύο μεθόδους 9, και τέλος η γαλλική μελέτη ACE πραγματοποιήθηκε μεταξύ 2003 και 2008 σε 25 κέντρα της Γαλλίας και συμπεριέλαβε 299 ασθενείς με ΑΚΑ > 5.0 εκ. 10
-Επιβίωση Ασθενών
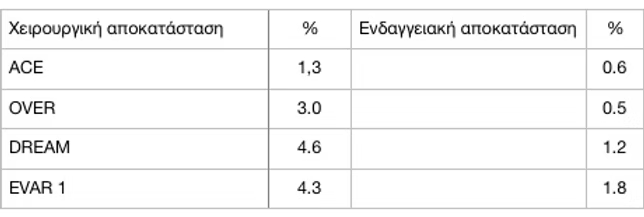
Η ανοικτή αποκατάσταση (ΟR) συνοδεύεται από υψηλότερη θνητότητα άμεσα μετεγχειρητικά σε σχέση με την ενδαγγειακή μέθοδο (Πίνακας). Εξαίρεση αποτελεί η μελέτη ACE που έδειξε μη στατιστικά σημαντική διαφορά μεταξύ των δυο τεχνικών αποκατάστασης του ΑΚΑ. Στη μελέτη DREAM, 2 έτη μετά την τυχαιοποίηση, η συνολική επιβιώση ήταν παρόμοια σε ασθενείς που υπεβλήθηκαν είτε σε ΧΑ είτε σε ΕΑ (89.6% και 89.7% αντίστοιχα). Το ίδιο ισχύει και 6 έτη μετά την τυχαιοποίηση (69,9% για την ΧΑ και 68,9% για την ΕΑ)11-12 Η μελέτη ACE ανέδειξε ικανοποιητικά αποτελέσματα επιβίωσης 3 έτη μετά την επέμβαση και για τις δύο ομάδες (85,1% για την ομάδα ΧΑ και 82,4% για την ομάδα ΕΑ, P=.24)10 Σε πρόσφατη δημοσίευση των αποτελεσμάτων της μελέτης OVER πρατηρήθηκε, επίσης, παρόμοια επιβίωση μετάξύ των ασθενών με ΧΑ και ΕΑ στα δύο έτη (μέση δίαρκεια ζωής 1,74 έτη για την ομάδα ΧΑ και 1,78 έτη για την ομάδα ΕΑ, P=.29)13
Σύγκριση Ανοικτής και Ενδαγγειακής – Θνητότητα 30 ημερών
Πίνακας: Αποτελέσματα τυχαιοποιημένων μελετών
Θνητότητα 30 ημερών
Νοσηρότητα – Ποιότητα ζωής
Στη μελέτη DREAM διαπιστώθηκε υπεροχή της ΕΑ σε σύγκριση με την ΧΑ κατά την πρώιμη μετεγχειρητική περίοδο. Μετά τους 6 μήνες από την επέμβαση, όμως, οι ασθενείς ανέφεραν καλύτερη ποιότητας ζωής μετά από ΧΑ παρά μετά από ΕΑ.14 Ανάλογα ευρήματα προέκυψαν και από τη μελέτη EVAR 1 καθώς διαπιστώθηκε καλύτερη ποιότητα ζωής έως και 12 μήνες μετά από ΕΑ, ενώ 4 έτη μετά την τυχαιοοποίηση δεν διαπιστώθηκαν διαφορές.15 Επιπροσθέτως, από τη μελέτη OVER13 αναδείχτηκε παρόμοια ποιότητα ζωής και στις δύο ομάδες ασθενών 2 ετη μετά την επέμβαση.
Σεξουαλική δυσλειτουργία
Τόσο η ΕΑ όσο και η ΧΑ συνδυάζονται με έκπτωση της σεξουαλικής δραστηριότητας κατά την πρώιμη μετγχειρητική περίοδο. Η αποκατάστη είναι πιο άμεση μετά από ΕΑ σε σύγκριση με την ΧΑ. Τα επίπεδα σεξουαλικής δραστηριότητας είναι παρόμοια και στις δύο μεθόδους μετά την πάροδο 3μηνου από την επέμβαση.9,16
Επανεπεμβάσεις
Αν και στα 2 έτη μετά την τυχαιοποίηση των ασθενών, στη μελέτη DREAM, το ποσοστό επιβίωσης χωρίς σοβαρές επιπλοκές είναι παρόμοιο (65,9% για την ΧΑ και 65,6% για την ΕΑ), στα 6 έτη παρατηρείται στατιστικα σημαντική υπεροχή της ΧΑ έναντι της ΕΑ (81,9% και 70,4%, P=0.03).12 Αξιοσημείωτο, επίσης, είναι ότι η πλειονότητα των επανεπεμβάσεων μετά από ΧΑ αφορούσαν σε αποκατάσταση μετγχειρητικής κοιλιοκήλης, ενώ οι επενεπεμβάσεις μετά από ΕΑ αφορούσαν σε επιπλοκές σχετιζόμενες με το ενδομόσχευμα (36/48). Η μελέτη ACE10, επιπλέον, ανέδειξε στατιστικά σημαντική διαφορά στο ποσοστό επανεπεμβάσεων (2,7% για την ΧΑ και 16,0% για την ΕΑ, Ρ < 0.0001) σε μέση περίοδο παρακολούθησης 3 έτη. Ακόμη και 8 έτη μετά την επέμβαση το ποσοστό των επανεπεμβάσεων είναι μεγαλύτερο μετά από ΕΑ σε σύγκριση με τη ΧΑ.17
Σε μια πρόσφατη μελέτη από τις ΗΠΑ, σε 19.2% από τους 1768 ασθενείς που είχαν υπεβλήθεί σε ΕΑ, απαιτήθηκε επανεπέμβαση για διόρθωση επιπλοκών σε μέσο χρονικό διάστημα παρακολούθησης 34μηνών. Αν και οι περισσότερες ΕΑ σχετιζόμενες επιπλοκές μπορούν να αντιμετωπιστούν με ενδοαυλικές μεθόδους με θνητότητα περίπου 3%, μετατροπή σε ανοικτή χειρουργική αποκατάσταση μπορεί να είναι υποχρεωτική για διάφορους λόγους κατά την πρώιμη ή την όψιμη μετεγχειρητική περίοδο.18 Σε μια τέτοια περίπτωση η θνητότητα ανέρχεται σε περίπου 10% για την πρώιμη μετατροπή και ξεπερνά το 25% για την όψιμη μετατροπή.19
Τα ανευρύσματα είναι μια ύπουλη πάθηση που πρέπει να διαγιγνώσκεται και να αντιμετωπίζεται πριν τη ρήξη ή την θρόμβωση. Η ενδαγγειακή μέθοδος πλεονεκτεί της ανοικτής χειρουργικής καθώς δεν απαιτεί πάντα γενική αναισθησία και συνοδεύεται με μειωμένη περιεγχειρητικά θνητότητα και νοσηρότητα. Ωστόσο, εμφανίζει αυξημένο ποσοστό απαιτούμενων επανεπεμβάσεων, σε σχέση με την ανοικτή μέθοδο και επιπλοκές που σχετίζονται συνήθως με το ενδομόσχευμα που τοποθετείται. Υπάρχει πάντα ο μικρός αλλά υπαρκτός κίνδυνος για την ενδαγγειακή μέθοδο, να μετατραπεί σε ανοικτή επέμβαση μέσα στην χειρουργική αίθουσα και χρήζει τακτικής παρακολούθησης μετεγχειρητικά με υπερήχους ή αξονική τομογραφία. Σε βάθος χρόνου η ενδαγγειακή μέθοδος, έχει τα ίδια ποσοστά θνητότητας με την ανοικτή μέθοδο. Η ανοικτή μέθοδος εξακολουθεί να αποτελεί την θεραπεία επιλογής σε νέους ασθενείς χαμηλού διεγχειρητικού κινδύνου με καλό προσδόκιμο επιβίωσης.
Βιβλιογραφία
1. Fleming C, Whitlock EP, Beil TL, Lederle FA. Screening for abdominal aortic aneurysm: a best-evidence systematic review for the U.S. Preventive Services Task Force. Ann Intern Med. 2005 Feb 1;142(3):203-11.
2. Dubost C, Allary M, Oeconomos N. Resection of an aneurysm of the abdominal aorta: reestablishment of the continuity by a preserved human arterial graft, with result after five months. AMA Arch Surg. 1952 Mar;64(3):405-8.
3. Volodos NL, Karpovich IP, Troyan VI, Kalashnikova Yu V, Shekhanin VE, Ternyuk NE, et al. Clinical experience of the use of self-fixing synthetic prostheses for remote endoprosthetics of the thoracic and the abdominal aorta and iliac arteries through the femoral artery and as intraoperative endoprosthesis for aorta reconstruction. Vasa Suppl. 1991;33:93-5.
4. Parodi JC, Palmaz JC, Barone HD. Transfemoral intraluminal graft implantation for abdominal aortic aneurysms. Ann Vasc Surg. 1991 Nov;5(6):491-9.
5. Eidt JF, Mills J, Rhodes RS, Biester T, Gahtan V, Jordan WD, et al. Comparison of surgical operative experience of trainees and practicing vascular surgeons: A report from the Vascular Surgery Board of the American Board of Surgery. Journal of vascular surgery : official publication, the Society for Vascular Surgery. 2011;53(4):1130-40.
6. Greenhalgh RM, Brown LC, Kwong GP, Powell JT, Thompson SG. Comparison of endovascular aneurysm repair with open repair in patients with abdominal aortic aneurysm (EVAR trial 1), 30-day operative mortality results: randomised controlled trial. Lancet. 2004 Sep 4-10;364(9437):843-8.
7. Endovascular aneurysm repair versus open repair in patients with abdominal aortic aneurysm (EVAR trial 1): randomised controlled trial. Lancet. 2005 Jun 25-Jul 1;365(9478):2179-86.
8. Prinssen M, Verhoeven EL, Buth J, Cuypers PW, van Sambeek MR, Balm R, et al. A randomized trial comparing conventional and endovascular repair of abdominal aortic aneurysms. N Engl J Med. 2004 Oct 14;351(16):1607-18.
9. Lederle FA, Freischlag JA, Kyriakides TC, Padberg FT, Matsumura JS, Kohler TR, et al. Outcomes Following Endovascular vs Open Repair of Abdominal Aortic Aneurysm. JAMA: The Journal of the American Medical Association. 2009 October 14, 2009;302(14):1535-42.
10. Jean-Pierre B. The ACE trial: A randomized comparison of open versus endovascular repair in good risk patients with abdominal aortic aneurysm. Journal of Vascular Surgery. 2009;50(1):222-4.
11. Blankensteijn JD, de Jong SECA, Prinssen M, van der Ham AC, Buth J, van Sterkenburg SMM, et al. Two-Year Outcomes after Conventional or Endovascular Repair of Abdominal Aortic Aneurysms. New England Journal of Medicine. 2005;352(23):2398-405.
12. De Bruin JL, Baas AF, Buth J, Prinssen M, Verhoeven EL, Cuypers PW, et al. Long-term outcome of open or endovascular repair of abdominal aortic aneurysm. N Engl J Med. 2010 May 20;362(20):1881-9.
13. Stroupe KT, Lederle FA, Matsumura JS, Kyriakides TC, Jonk YC, Ge L, et al. Cost-effectiveness of open vs endovascular repair of abdominal aortic aneurysm: Results of a multicenter randomized trial. Journal of vascular surgery : official publication, the Society for Vascular Surgery. 2012.
14. Prinssen M, Buskens E, Blankensteijn JD, On behalf of the Dtp. Quality of Life after Endovascular and Open AAA Repair. Results of a Randomised Trial. European journal of vascular and endovascular surgery : the official journal of the European Society for Vascular Surgery. 2004;27(2):121-7.
15. Endovascular aneurysm repair versus open repair in patients with abdominal aortic aneurysm (EVAR trial 1): randomised controlled trial. The Lancet.365(9478):2179-86.
16. Prinssen M, Buskens E, Tutein Nolthenius RP, van Sterkenburg SMM, Teijink JAW, Blankensteijn JD. Sexual Dysfunction After Conventional and Endovascular AAA Repair: Results of the DREAM Trial. Journal of Endovascular Therapy. 2004 2004/12/01;11(6):613-20.
17. Endovascular versus Open Repair of Abdominal Aortic Aneurysm. New England Journal of Medicine. 2010;362(20):1863-71.
18. Mehta M, Sternbach Y, Taggert JB, Kreienberg PB, Roddy SP, Paty PSK, et al. Long-term outcomes of secondary procedures after endovascular aneurysm repair. Journal of Vascular Surgery. 2010;52(6):1442-9.
19. Moulakakis KG, Dalainas I, Mylonas S, Giannakopoulos TG, Avgerinos ED, Liapis CD. Conversion to open repair after endografting for abdominal aortic aneurysm: a review of causes, incidence, results, and surgical techniques of reconstruction. J Endovasc Ther. 2010 Dec;17(6):694-702.



